獲悉陸軍軍醫大學新橋醫院檢驗醫學中心李忠俊教授團隊的研究論文《Single-cell profiling of ANKRD26 thrombocytopenia reveals progenitor expansion and polyploid apoptosis via JUNB-p21》近日在國際頂級血液學期刊《Blood》(影響因子23.1)正式發表,闡明瞭Ⅱ型遺傳性血小板減少症的發病新機制,不僅為該病的精準治療及藥物研發提供了全新靶點和思路,更為血小板再生提供了新的策略。《Blood》雜誌同期配發評論員文章對該研究給予高度評價,明確指出其成功破解了困擾醫學界十五年的臨牀悖論。

据了解,Ⅱ型遺傳性血小板減少症,是一種遺傳性血液病,患者面臨終身出血風險及發展為血液腫瘤的潛在威脅。自2011年該病的致病基因是ANKRD26被確定以來,臨牀觀察中出現了一個長期無法解釋的悖論:患者骨髓裡產生血小板的母細胞——巨核細胞數量非但不少,反而時常增多,但外周血小板計數卻持續低下。由於巨核細胞極其稀少、脆弱且難以在體外真實模擬,這一悖論背後真正的原因,全球科學家一直無法精準解析。
為揭開真相,李忠俊教授團隊聯閤中國醫學科學院血液學研究所楊仁池教授團隊和美國加利福尼亞大學Shengwen Calvin Li教授團隊,對4名患者原代造血幹祖細胞與巨核細胞的數萬個單細胞數據進行了分析,結合流式細胞技術和免疫熒光技術,精準鎖定了致病蛋白ANKRD26在細胞內的活動軌跡。
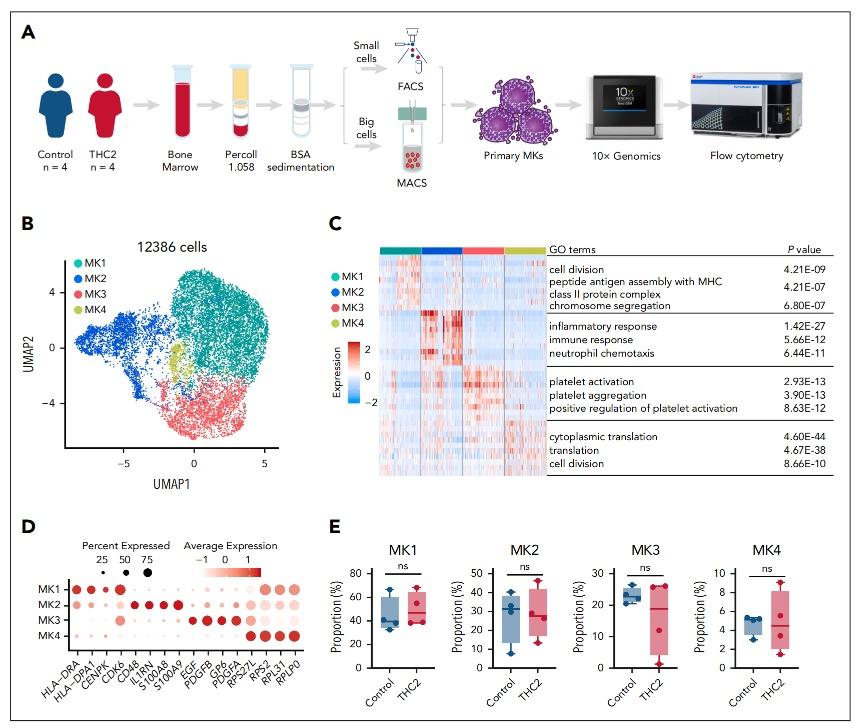
研究發現,ANKRD26蛋白在細胞發育的不同階段扮演了完全不同的角色:早期,ANKRD26像一劑“生長燃料”,促進巨核祖細胞增殖,讓骨髓裡產生更多的“種子細胞”;晚期隨着巨核細胞的成熟和多倍體形成,它卻變身為“毀滅者”,定位到多倍體細胞的數量增多的中心體位置,激活了一條新的JUNB-p21細胞自殺信號通路,導致這些本該生成血小板的母細胞在還沒完成任務前就成批“自殺性”凋亡。正是這種“先促進後摧毀”的矛盾機制,解釋了為何患者骨髓裡的巨核細胞看似正常甚至增多,卻無法有效生成血小板。該研究闡明的分子靶標有望成為未來藥物開發的新靶點,為ANKRD26相關血小板減少症患者帶來實現精準治療的新希望。
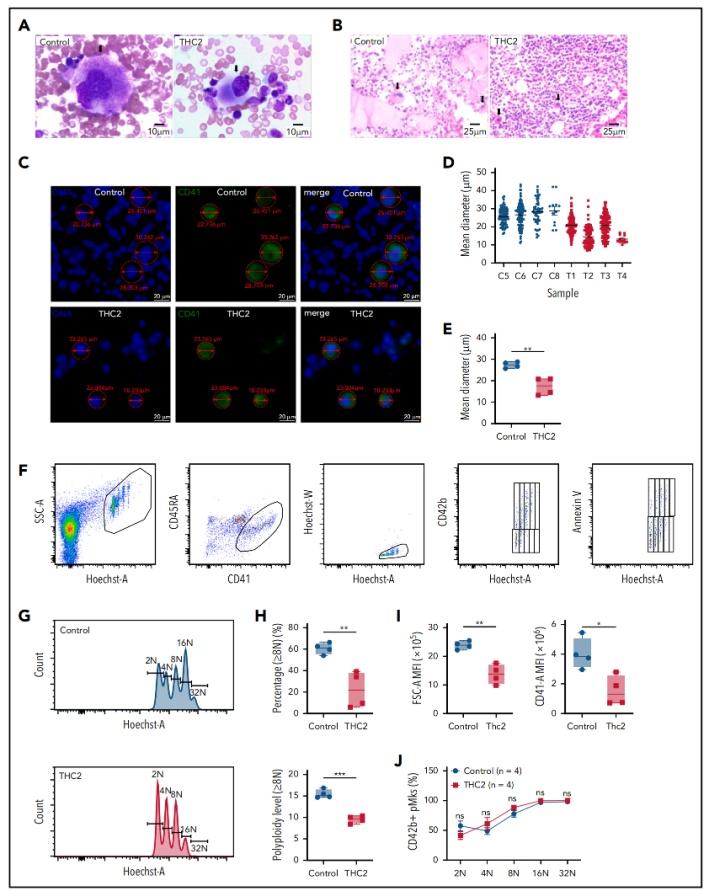
記者在採訪中了解到,該研究由新橋醫院檢驗醫學中心李忠俊教授領銜,中心冉茜特聘教授、中國醫學科學院血液病醫院楊仁池教授以及美國加利福尼亞大學Shengwen Calvin Li教授作為共同通訊作者,中心陳立副教授、胡藍月實驗師與中國醫學科學院血液病醫院劉曉帆主任醫師作為共同第一作者完成。







 今日熱搜
今日熱搜















 查看更多
查看更多















