香港大學(港大)科研團隊在細胞微管研究取得重大突破,首次揭示微管蛋白如何透過機械力學感應控制細胞活動。這項由港大工程學院機械工程系林原教授與港大李嘉誠醫學院生物醫學學院狄士傑教授共同領導的研究,為理解細胞“骨架”運作機制帶來新見解。

微管作為細胞骨架核心組件,是由微管蛋白異二聚體組成的中空管狀結構,不僅維持細胞形態,更參與物質運輸等關鍵生理過程。微管需要與多種蛋白質相互作用——部分作用於微管外表面,另一些則作用於其管腔。儘管微管外表面易於接近,但管腔結合蛋白如何進入受限的微管內腔仍是未解之謎。研究團隊運用跨學科研究方法,結合生物、物理學、機械工程等技術,成功破解微管“門控”之謎。
狄士傑教授團隊透過“單分子螢光生物檢測”配合機械儀器操作(圖1),發現微管蛋白亞型(即微管蛋白的不同變體)作為力感應元件能夠調控微管管腔可及性,從而使得酶與微管內腔表面發生相互作用。
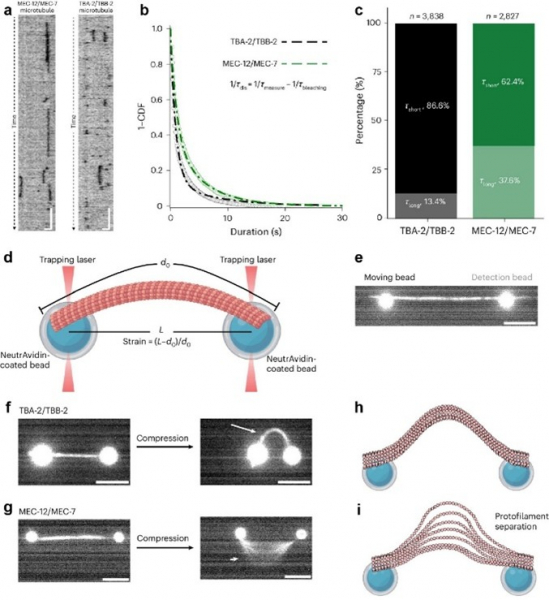
研究團隊利用三維電腦模擬技術構建微管精細模型,發現特定微管蛋白亞型因橫向相互作用較弱,在機械外力作用下可產生納米級縫隙(圖2)。
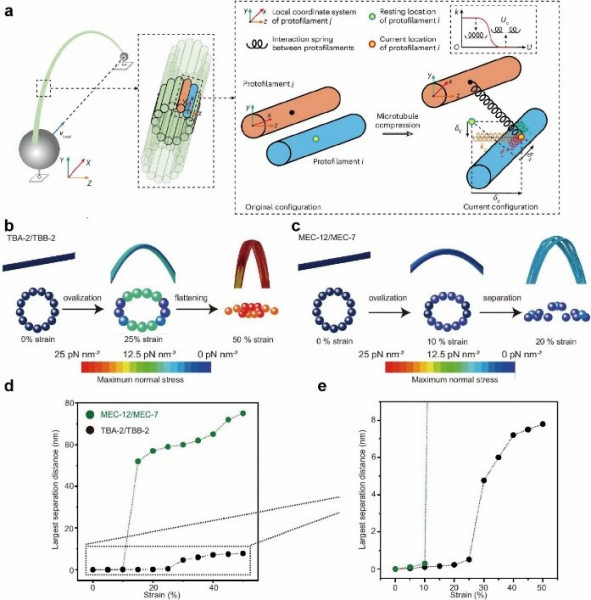
林教授指出:“實驗證實,這些縫隙的大小恰到好處,足以讓管腔結合蛋白等關鍵物質進出,猶如細胞內的智能開關。”研究分析顯示,不同微管蛋白亞型的組合能精確調控微管的機械特性,使其能夠差異化響應熱力波動或外界機械刺激。這種動態調節機制解釋了細胞如何靈活適應環境變化,突破物理限制並維持內部物質運輸的穩定性。
林原教授與狄士傑教授表示:“此項研究不僅加強我們對細胞機械轉導現象的理解,未來還有望為先進活性生物材料的研發提供關鍵線索。”
研究成果已發表於《自然-物理》(Nature Physics),文章標題為“Tubulin isotypes of C. elegans harness the mechanosensitivity of the lattice for microtubule luminal accessibility”。







 今日熱搜
今日熱搜














 查看更多
查看更多















